关于人类免疫缺陷病毒(HIV)如何管理和组装其脂质包膜的新见解已经被RIKEN生物学家收集。这些关于HIV生物学的发现有助于为寻找新的治疗方法提供信息。这篇论文发表在《自然通讯》杂志上。
一套精心挑选的服装可以打开人类世界的大门。HIV也是如此,它把自己包裹在一层特殊的脂质外衣中,这极大地影响了它进入和随后退出宿主细胞的能力。
像大多数病毒一样,艾滋病毒只有一组基本的基本基因,并且缺乏细胞中存在的几乎所有代谢功能。
“由于病毒不能合成脂质,艾滋病毒从宿主细胞的质膜上‘窃取’脂质,”理研综合脂质学先驱项目的Toshihide Kobayashi解释说。
然而,这种膜的生化组成明显不同于病毒包膜,病毒包膜富含两种类型的脂质:胆固醇和鞘磷脂。
当新复制的病毒从感染细胞的膜“芽”出来时,一种叫做Gag的病毒蛋白促进了这些脂质的聚集,但其潜在的机制尚不清楚。
为了弄清这个谜团的深度,小林与法国斯特拉斯堡大学(University of Strasbourg)的研究人员合作,他在那里也有一个实验室。
HIV Gag蛋白的表达足以在培养的人类细胞中驱动质膜出芽,研究小组使用了一种复杂的多管齐下的成像策略来观察这一过程。
“我们的实验室一直在开发和表征与特定脂质结合的蛋白质,”小林说。研究小组用荧光染料标记鞘磷脂和胆固醇结合蛋白。然后,他们用尖端的显微镜方法观察了这些脂质在gag诱导出芽过程中的行为,这种方法可以分解单个分子。
质膜由两层组成:内小叶和外小叶(根据它们相对于细胞内部的位置命名)。
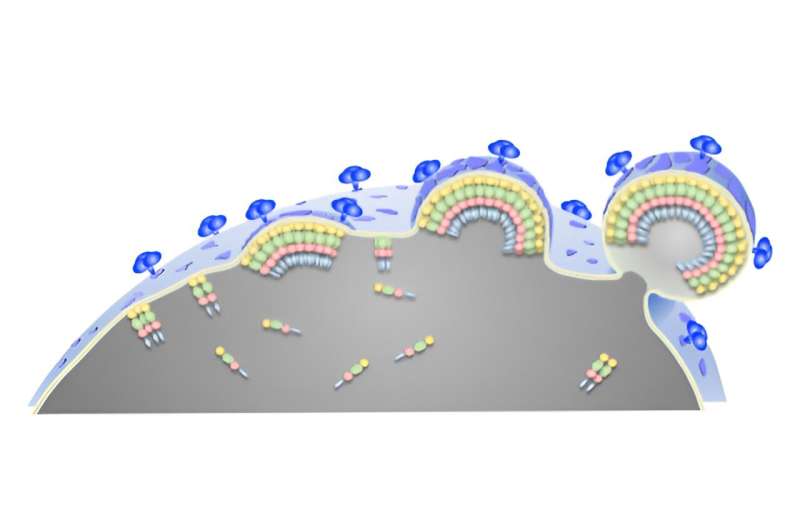
研究人员观察到,当Gag附着在内小叶上时,它与外小叶上的胆固醇和鞘磷脂岛重叠,物理上隔离了这些脂质。随着越来越多的Gag蛋白与小叶结合并相互作用,鞘磷脂的积累继续增加。
因此,膜的附近表面开始弯曲,进一步集中这些脂质结构域,作为出芽过程最后阶段的前奏。
这些发现是了解HIV生物学的重要一步,但关键问题仍然存在。小林说:“我们已经证明,内部的小叶蛋白重组了外部的小叶脂质,但我们不知道是如何重组的。”“我们的首要任务是澄清这一机制。”











