在这项工作中,我们研究了5型腺苷酸环化酶(AC5)在给予牙龈卟啉单胞菌脂多糖(PG-LPS)的小鼠诱导的心功能障碍中的作用,其剂量相当于牙周炎(PD)患者的循环水平。与对照组相比,给予PG-LPS的小鼠心功能明显下降,但用AC5抑制剂阿糖腺苷治疗1周后,功能障碍得到改善。PG-LPS组心肌纤维化和心肌细胞凋亡明显增加,但阿糖腺苷阻断了这些变化。pg - lps诱导的心功能障碍与环AMP/Ca2+-钙调素依赖性蛋白激酶II信号的激活和苏氨酸17磷酸化增加有关。这些结果表明,AC5药物抑制可能是治疗pd相关心血管疾病的一种有希望的方法。
日本牙科协会将口腔虚弱定义为口腔功能下降,同时伴有精神和身体功能下降[1]。最近一项针对2044名日本老年人的队列研究发现,口腔虚弱的人比没有口腔虚弱的人有更高的身体虚弱需要护理和死亡的风险[2]。有趣的是,一项大规模流行病学调查发现,心血管疾病(CVD)患者发生口腔健康问题的风险高于社区居民[3,4]。口腔健康状况不佳,如牙周炎(PD)、牙齿缺失和牙齿咬合能力丧失,与未来CVD风险增加两倍以上相关[3,4]。此外,由于厌食症或肠道水肿、细胞因子诱导的分解代谢和心脏恶病质,CVD患者营养不良的发生率很高[5]。然而,口腔健康问题和心血管疾病之间的纵向关系尚不清楚。
CVD是导致身体虚弱和死亡的主要原因,慢性刺激交感神经系统是患者CVD的常见原因[6]。腺苷酸环化酶(Adenylyl cyclase, AC)是β-肾上腺素能受体(β-AR)信号刺激的靶酶[7]。哺乳动物中AC有九种主要的亚型,其中5型AC (AC5)是成人心脏中主要的亚型[8,9,10]。我们开发了一种AC5破坏的小鼠模型[11,12,13],我们还发现抗病毒药物阿糖腺苷是小鼠心脏AC的抑制剂[14]。在这项工作的基础上,我们发现基因和药理学上的AC5抑制可能与抵抗心血管疾病发展和延长寿命有关[15]。我们最近也提出证据表明,咬合不和谐诱导的心脏纤维化和心肌细胞凋亡可能是由烟酰胺腺嘌呤二核苷酸磷酸氧化酶4 (NOX4)通过激活AC5而产生的活性氧(ROS)引起的。NOX4的活性受其表达水平的调节[16],因此在本研究中,我们检测了在给予或不给予阿糖腺苷的牙龈卟啉单胞菌脂多糖(PG-LPS)的小鼠心脏中NOX4蛋白的表达。
PD是一种严重的口腔健康问题,甚至可导致牙齿脱落和牙合能力丧失,其治疗可通过减少氧化应激提高对CVD发展的抵抗力和延长寿命[17,18]。在这种情况下,我们已经证明,持续亚临床暴露于PG-LPS可通过激活环AMP (cAMP)-蛋白激酶A (PKA)和Ca2+/钙调素依赖性蛋白激酶II (CaMKII)信号诱导心肌细胞损伤和心力衰竭[18]。由于大多数Ca2+处理蛋白的磷酸化在许多实验性心力衰竭模型中被改变,这可能导致Ca2+泄漏增加,我们还研究了PG-LPS处理对磷蛋白(PLN)在Thr-17位点磷酸化的影响,已知这是由CaMKII介导的[19]。
AC5在pg - lps介导的心脏重构和功能障碍中的作用尚不清楚。然而,先前关于小鼠和PG-LPS治疗小鼠AC5缺乏症的报道表明,阿糖腺苷抑制心脏AC亚型可能会预防PG-LPS治疗小鼠的心肌细胞损伤和心力衰竭,其剂量相当于亚临床PD的水平。重要的是,阿糖腺苷作为抗病毒药物已在人类中使用多年[14]。因此,阿糖腺苷,而不是β受体阻滞剂,可能是一种安全的,临床可立即获得的药物,用于治疗或预防PG-LPS诱导的心功能障碍。
因此,本研究的目的是研究阿糖腺苷抑制AC5对PG-LPS治疗小鼠心功能、心脏纤维化和心肌细胞凋亡的影响,其剂量相当于PD患者的循环水平,并阐明其中的机制。
所有实验均在CLEA Japan (Tokyo, Japan)提供的12周龄雄性C57BL/6小鼠身上进行。按照本组小鼠研究的标准条件[20,21,22],将小鼠置于23°C下,12-12个明暗循环,上午8:00开灯。食物和水都是免费供应的。
PG-LPS (# 14966 - 71;将Invivogen, San Diego, CA, USA)溶解于磷酸盐缓冲盐水(PBS, pH=7.5)中配制成0.6 mg/mL的原液[23],并根据所需剂量(PG-LPS: 0.8 mg/kg)将适当体积的该溶液加入0.2 mL的PBS中配制成腹腔注射溶液(每天1次,连续1周)。将小鼠分组饲养(每笼约3只),并分为四组:正常对照组(control)、PG-LPS处理组、仅阿糖腺苷处理组和PG-LPS加阿糖腺苷处理组(PG-LPS +阿糖腺苷)(图1a)。长期输注溶解在DMSO中的阿糖腺苷(#359-13471);Sigma, St. Lois MO, USA)以15 mg/kg/天的剂量进行1周,通过渗透微型泵输送(2002型;ALZET, Cupertino, CA, USA)[15,21,24]。阿糖腺苷的剂量(15mg /kg/天;(经批准用于人类临床使用的剂量)的选择是基于先前研究使用的剂量:该剂量不会消除急性异丙肾上腺素的肌力效应,不会在基线时抑制心功能,并保留对AC5的高选择性[15]。在为期一周的实验期间监测体重(BW)(对照组:n=6, PG-LPS: n=7,阿糖腺苷:n=6, PG-LPS +阿糖腺苷:n=7)(图1b)。本研究中使用的PG-LPS剂量与PD患者的循环水平一致,表明该模型不是脓毒症模型,确实没有观察到死亡[23]。治疗结束后,用异氟醚(1.0-1.5% v/v)麻醉小鼠,颈椎脱臼致死[25]。切除心脏、肺和肝脏,称重,液氮冷冻,- 80°C保存。脏器质量(mg)与胫骨长度(TL)之比;mm)作为脏器体积指标(图1c-e)。所有动物实验均符合ARRIVE指南[26],并按照美国国立卫生研究院(National Institutes of Health)的实验动物护理和使用指南[27]和机构指南进行。
图1
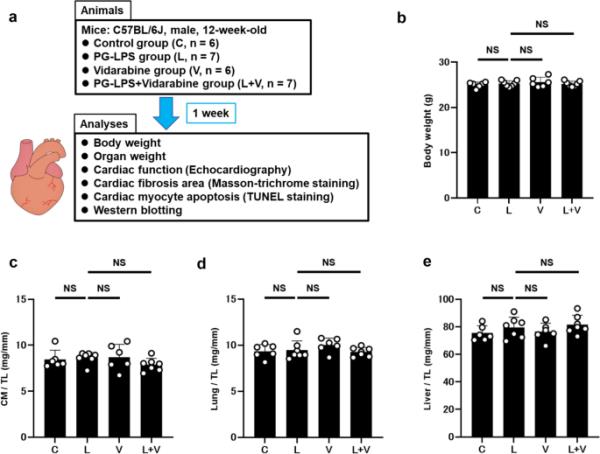
实验过程示意图及体重、心肌重量、肺重量和肝脏重量的比较。将12周龄雄性C57BL/6小鼠分为4组:正常对照组(control)、PG-LPS处理组(L)、阿糖腺苷处理组(V)、PG-LPS +阿糖腺苷处理组(L + V)。以15mg /kg/天的剂量,通过微型渗透泵慢性输注阿糖腺苷1周,并进行指示测量。b对照组、PG-LPS组、阿糖腺苷组和PG-LPS +阿糖腺苷组体重相近。NS,与对照组无显著差异(P > 0.05)。单因素方差分析,然后进行Tukey事后检验)。c四组小鼠输注PG-LPS后1周心脏(c)、肺(d)和肝脏大小(重量/胫骨长度(TL)比(mg/mm))无显著差异。P=NS,与对照组无显著差异。单因素方差分析后进行Tukey事后检验)。数据以均数±标准差表示,散点表示单个数据
用异氟烷蒸汽(1.0-1.5% v/v)麻醉小鼠,以维持尽可能轻的麻醉,超声心动图测量采用超声仪(TUS-A300, Toshiba, Tokyo, Japan),如前所述[19]。
所有左心室(LV)尺寸都表示为四个连续选择的节拍的平均值。心率(HR)由记录在m模式示踪上的心循环确定,使用至少连续三次心跳。其他参数由m模导出的LV维数采用Teichholz公式计算[28]:
EDV (mL):左室舒张末期容积;ESV (mL):左心室收缩末容积;LVIDd (mm):舒张末期左室内径;LVIDs (mm):收缩末期左心室内部尺寸。
野生型对照(12周龄C57BL/6小鼠)采用Teichholz公式计算的所有LV维度与我们[20]和另一组[29]的研究报告一致。
跨教派。(10 μm) (Control;n=6;PG-LPS;n=7;阿糖腺苷;n=6;PG-LPS +阿糖腺苷;n=6)用低温恒温器(CM1900, Leica microsystems, Nussloch, Germany)在- 20°C下切割。将切片风干,用4%多聚甲醛(v/v)在0.1 M PBS中固定[30,31,32]。
间质纤维化采用masson -三色染色,使用Accustatin三色染色试剂盒(#HT15-1KT;Sigma),按照制造商的方案,如前所述[19,33]。使用图像分析软件(图J 1.45)对间质纤维化区域进行量化,评估masson -三色切片中蓝色区域的百分比[19]。
采用细胞凋亡原位检测试剂盒(#293-71501;Wako,大阪,日本)。人工统计4组6个切片每视野tunel阳性核数(对照组;n=4;PG-LPS;n=4;阿糖腺苷;n=4;PG-LPS +阿糖腺苷;n=5)在20倍的显微镜下,取平均值,表示为tunel阳性核的比率(%)[12,19]。将总细胞核和tunel阳性细胞核的计数限制在肌细胞真实横截面的区域,可以选择性地只计数那些明确位于肌细胞内的细胞核。
从小鼠身上切除心肌(对照组;n=6;PG-LPS;n=7;阿糖腺苷;n=6;PG-LPS +阿糖腺苷;n=7)(图1a)用Polytron (Kinematica AG, Lucerne, Switzerland)在冰冷的RIPA缓冲液(#89900;Thermo Fisher Scientific, Waltham, MA, USA: 25 mM Tris-HCl (pH 7.6), 150 mM NaCl, 1% NP-40, 1%脱氧巧克力酸钠,0.1% SDS),添加Halt?蛋白酶抑制剂鸡尾酒,EDTA-free (#87785;Thermo Fisher Scientific),匀浆在13000 g下在4°C下离心10分钟。收集上清液,使用DC蛋白测定试剂盒(Bio-Rad, Hercules, CA, USA)测定蛋白浓度。等量的蛋白质(5 μg)进行sds -聚丙烯酰胺凝胶电泳,并印迹到0.2 mm PVDF膜上(Millipore, Billerica, MA, USA)。
Western blotting采用市售抗体[11,12,19],针对α-平滑肌肌动蛋白(α-SMA) (1:1000, #19245), CaMKII (1:1000, #3362), phospho-CaMKII (1:1000, Thr-286, #3361)和B细胞淋巴瘤2 (BCL-2)(1:1000, #3498)[来自cell Signaling Technology (Boston, MA, USA)],甘油醛3-磷酸脱氢酶(GAPDH) (1:20 00, sc-32233)[来自Santa Cruz Biotechnology (Santa Cruz, CA, USA)], phospho-phospholamban (PLN) (1:5000, Thr-17),#A010-13)和PLN (1:5000, #A010-14)[来自Badrilla(英国利兹)],NOX4 (1:1000, #ab133303)[来自Abcam(英国剑桥)],AC5 (1:1000, #SAB4500206)[来自Sigma]和氧化CaMKII (Met-281/282)(1:1000, #07-1387)[来自Millipore(美国马萨诸塞州Billerica)]。采用购自GB Healthcare (Amersham, UK)的辣根过氧化物偶联抗兔IgG (1:50 000, #NA934)或抗小鼠IgG (1:50 000, #NA931)作为二抗。一抗体和二抗体用tris缓冲盐水(pH 7.6)稀释,溶液中添加0.1% Tween 20和5%牛血清白蛋白。用增强化学发光溶液(ECL: Prime Western Blotting Detection Reagent)对斑点进行显像,并用密度计(ASL-600, GE Healthcare, Piscataway, NJ, USA,或LAS-1000, Fuji Photo Film, Tokyo, Japan)扫描。请注意,不同的western blotting图(图2c, 4a-e)中有不同数量的样本,因为我们排除了异常值(与同一组中的其他值相比,极低或极高的值)。
图2
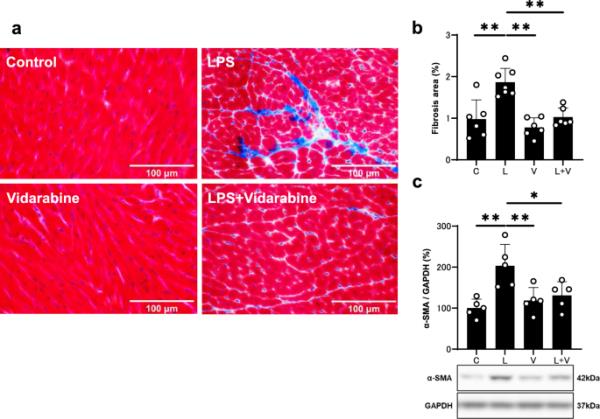
阿糖腺苷对pg - lps诱导的心脏纤维化的影响。a对照组(左上)、PG-LPS组(右上)、阿糖腺苷组(左下)和BO +阿糖腺苷组(右下)心肌马松三色染色切片的代表性图像。标尺:100 μm。b PG-LPS组纤维化面积明显增加(n=7, **P < 0.01), PG-LPS +阿糖腺苷组纤维化面积明显增加(n=6, **P < 0.01)。单因素方差分析,然后进行Tukey事后检验)。PG-LPS组心肌组织中纤维化相关基因α-SMA的表达显著升高(n=5, **P < 0.01),而PG-LPS +阿糖腺苷组心肌组织中α-SMA的表达被抑制(n=5, *P < 0.05)。单因素方差分析,然后进行Tukey事后检验)。免疫印迹的全尺寸图像见附加文件1:图S1。数据以均数±标准差表示,散点表示单个数据
数据显示平均值±标准差(SD)。数据比较采用单因素方差分析,然后进行Tukey事后检验。当P < 0.05时认为差异有统计学意义。
摘要
背景
材料与方法
结果
讨论
结论
数据和材料的可用性
缩写
参考文献
致谢
作者信息
道德声明
补充信息
搜索
导航
#####
对照组、PG-LPS组、阿糖腺苷组、PG-LPS +阿糖腺苷组在输注PG-LPS后1周体重相似(PG-LPS [n=7]: 25.2±0.7,阿糖腺苷[n=6]: 25.6±1.1,PG-LPS +阿糖腺苷[n=7]: 25.2±0.6 g,差异均无统计学意义;P > 0.05]与对照组比较[n=6;25±0.6 g])(图1b)。
我们还研究了加/不加阿糖滨的PG-LPS对心脏大小的影响,即每TL心肌质量(mg/mm)(图1c)和对每TL湿肺和肝重量的影响(图1d, e)。四组之间得到了类似的结果。
因此,本实验中使用的剂量的PG-LPS和阿糖腺苷在1周的实验期间都没有影响生长、心脏肥厚或肺/肝充血。
我们通过超声心动图(表1)来评估EF和%FS的心功能。与对照组相比,PG-LPS组两项指标均显著降低(EF: control [n=6] vs. PG-LPS [n=7]: 67±1.0 vs. 61±0.9%,P < 0.01;% FS:控制(n=6)与PG-LPS (n=6): 32±0.8 vs . 28±0.6%,P < 0.01)。单独使用阿糖腺苷[n=6]对EF和%FS无影响,但阻断了PG-LPS诱导的1周EF和%FS的下降(EF: PG-LPS [n=7] vs. PG-LPS +阿糖腺苷[n=6]: 61±0.9 vs. 67±1.4%,P < 0.05;% FS: PG-LPS (n=7)与PG-LPS +阿糖腺苷(n=6): 28±0.6 vs . 32±0.9%,P < 0.05)。
表1 PG-LPS治疗后1周超声心动图心功能评估
这些数据表明,PG-LPS治疗至少部分通过激活AC5来降低心功能。
我们通过马松三色染色检测了加/不加阿糖滨的PG-LPS对心肌纤维化的影响(图2a)。PG-LPS治疗显著增加心肌纤维化面积(对照[n=6]与PG-LPS [n=7]: 0.98±0.46 vs. 1.86±0.34%,经单向方差分析和Tukey事后检验,P < 0.01),与我们之前的研究结果一致[18,20](图2b)。单独使用阿糖腺苷不改变纤维化面积,但阻断了PG-LPS诱导的纤维化增加(PG-LPS [n=6] vs. PG-LPS +阿糖腺苷[n=7]: 1.86±0.34 vs. 1.03±0.22%,经单向方差分析和Tukey事后检验P < 0.05)(图2b)。
我们还通过测量PG-LPS开始后1周α-SMA表达水平来评估心肌纤维化,因为该参数与心肌纤维化密切相关[31,34]。α的表达水平sma明显增加心肌PG-LPS-treated老鼠(控制(n=5)与PG-LPS (n=5): 100±22和203±52%,P < 0.01单向方差分析之后,图基的事后考验),和增加显著抑制阿糖腺苷(PG-LPS (n=5)与PG-LPS +阿糖腺苷(n=5): 203±52和131±33%,P < 0.01单向方差分析其次是图基的事后测试)(图2 c和额外的文件1:图S1)。
接下来,我们通过TUNEL染色检测了加/不加阿糖滨的pg - lps处理小鼠心肌细胞的凋亡情况(图3a)。PG-LPS处理显著增加细胞凋亡(对照组[n=4] vs. PG-LPS [n=4]: 1.5±0.9 vs. 6.4±2.2%,经单因素方差分析和Tukey事后检验P < 0.01)。单独使用阿糖腺苷(n=4)对tunel阳性心肌细胞的数量没有影响,但它阻断了PG-LPS诱导的tunel阳性心肌细胞的增加(PG-LPS [n=4] vs. PG-LPS +阿糖腺苷[n=5]: 6.4±2.2 vs. 2.8±1.6%,经单向方差分析和Tukey事后检验,P < 0.05)(图3b)。
图3
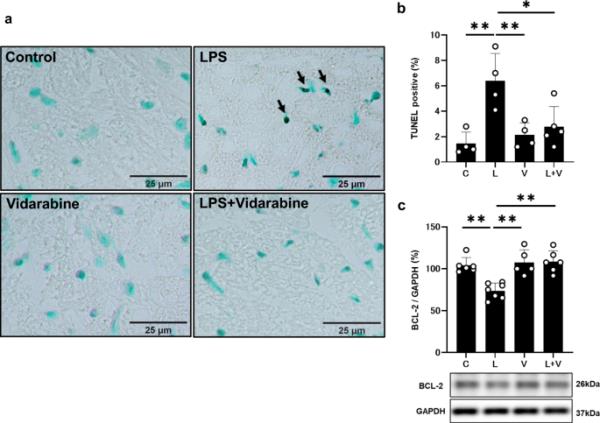
阿糖腺苷对pg - lps诱导心肌细胞凋亡的影响。a对照组(左上)、PG-LPS(右上)、阿糖腺苷(左下)和PG-LPS +阿糖腺苷(右下)组心肌tunel染色切片的代表性图像。比例尺:25 μm。b PG-LPS组tunel阳性肌细胞数量明显增加(n=4, **P < 0.01), PG-LPS +阿糖腺苷组tunel阳性肌细胞数量明显减少(n=5, **P < 0.01)。单因素方差分析,然后进行Tukey事后检验)。PG-LPS组大鼠心肌中抗凋亡BCL-2蛋白c表达显著降低(n=7, **P < 0.01),而PG-LPS +阿糖腺苷组大鼠心肌中抗凋亡BCL-2蛋白c表达明显受阻(n=5, *P < 0.05)。单因素方差分析,然后进行Tukey事后检验)。免疫印迹的全尺寸图像见附加文件1:图S2。数据以均数±标准差表示,散点表示单个数据
我们还通过测量心脏细胞凋亡调节剂BCL-2的变化来评估心肌细胞的凋亡(图3c和附加文件1:图S2)。PG-LPS处理小鼠心肌BCL-2表达显著降低(对照[n=6] vs. PG-LPS [n=7]: 100±9.3 vs. 74±9.3%,单因素方差分析加Tukey事后检验P < 0.01),阿糖腺苷处理小鼠心肌BCL-2表达显著降低(PG-LPS [n=7] vs. PG-LPS +阿糖腺苷[n=6]: 74±9.3 vs. 109±13%,单因素方差分析加Tukey事后检验P < 0.01)。
AC5表达升高在慢性儿茶酚胺应激引起的心力衰竭中已被证实[13]。因此,我们检测了AC5在心脏中的表达,发现四组之间的表达水平相似(图4a和附加文件1:图S3)。
图4
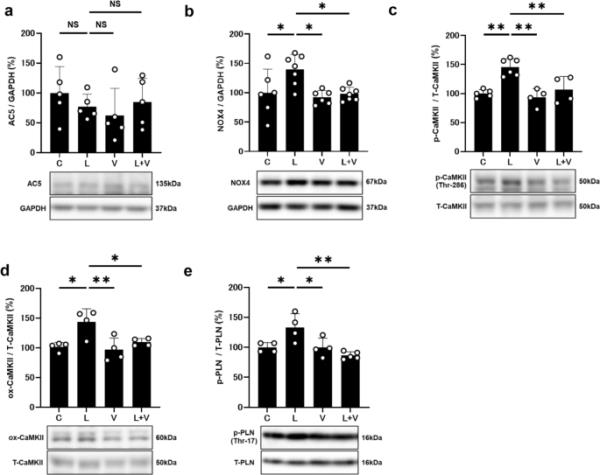
阿糖腺苷对AC5、NOX4、p-CaMKII、ox-CaMKII和磷酸化- pln的影响。a四组心肌组织中AC5表达相似。NS;差别不大。采用单因素方差分析。通过Tukey的事后检验)免疫印迹的全尺寸图像显示在附加文件1:图S3。b NOX4在PG-LPS组心肌组织中的表达显著升高(n=7, *P < 0.05),而在PG-LPS +阿糖腺苷组中,NOX4的表达被显著阻断(n=7, *P < 0.05)。单因素方差分析,然后进行Tukey事后检验)。免疫印迹的全尺寸图像见附加文件1:图S4。phospho-CaMKII (Thr-286) c表达量在PG-LPS组显著升高(n=6, **P < 0.01),在PG-LPS +阿糖腺苷组显著降低(n=7, **P < 0.01)。单因素方差分析,然后进行Tukey事后检验)。免疫印迹的全尺寸图像见附加文件1:图S5。氧化camkii (ox-CaMKII)表达量在PG-LPS组显著升高(n=4, *P < 0.01),在PG-LPS +阿糖腺苷组显著降低(n=4, *P < 0.05)。单因素方差分析后进行Tukey-Kramer事后检验。免疫印迹的全尺寸图像见附加文件1:图S6。磷酸化- pln (Thr-17)表达量在PG-LPS组显著升高(n=4, *P < 0.05),在PG-LPS +阿糖腺苷组显著降低(n=5, *P < 0.01)。单因素方差分析,然后进行Tukey事后检验)。免疫印迹的全尺寸图像见附加文件1:图S7。数据以均数±标准差表示,散点表示单个数据
PG-LPS处理组NOX4表达显著升高(对照组[n=6] vs. PG-LPS [n=7]: 100±40.2 vs. 140±25.9%,P < 0.05 vs.对照组),阿糖腺苷抑制了NOX4表达的升高(PG-LPS [n=7] vs. PG-LPS +阿糖腺苷[n=7];(140±25.9 vs. 98±11.6%,P < 0.05 vs. PG-LPS)(图4b和附加文件1:图S4)。
CaMKII在ROS存在下通过磷酸化和氧化被激活,参与心脏重塑和功能障碍的发展[35]。因此,我们检查了四组心脏中磷酸化CaMKII (Thr-286)(图4c和附加文件1:图S5)和氧化甲硫氨酸- 282camkii (ox-CaMKII)的数量(图4d和附加文件1:图S6),发现它们在PG-LPS处理后1周显著增加(磷酸化CaMKII (Thr-286):对照组[n=5]与PG-LPS [n=6]: 100±6.9比146±14.6%,P < 0.01与对照组相比;ox-CaMKII:控制(n=4)与PG-LPS [n=4]: 100±7.5 vs 143±22.4%,P < 0.05与控制)。阿糖腺苷(phospho-CaMKII (Thr-286)): PG-LPS [n=6] vs. PG-LPS +阿糖腺苷[n=4]显著减弱这些变化;146±14.6%比107±22.6%,P < 0.01;ox-CaMKII: PG-LPS (n=4)与PG-LPS +阿糖腺苷(n=4);143±22.4 vs 110±6.3%,P < 0.05 vs PG-LPS)。
PG-LPS治疗组心脏磷酸化- pln (Thr-17)显著升高(对照组[n=4] vs. PG-LPS [n=4]: 100±7.9 vs. 133±22%,P < 0.05 vs.对照组)。阿糖腺苷(PG-LPS [n=4] vs. PG-LPS +阿糖腺苷[n=5])显著减弱了这种增加;133±22 vs. 86±6.1%,P < 0.01 vs. PG-LPS)(图4e和附加文件1:图S7)。
下载原文档:https://link.springer.com/content/pdf/10.1186/s12576-023-00873-5.pdf











