利用猪作为器官供体已经将异种移植技术发展到几乎可以用于临床的地步。然而,仍然存在与异种移植相关的人畜共患风险,并且需要调查猪内源性逆转录病毒的潜在传播。尽管有大量尝试消除这种风险,但通过选择PERV- c低表达的猪,以及使用CRISPR/Cas9对PERV进行全基因组失活,没有研究重复感染抗性(SIR)的影响。SIR是一种防止再感染(重复感染)的病毒特性。对于PERV,潜在的机制尚不清楚,是否以及如何保护携带功能性PERV的细胞。我们以PERV-C(5683)为参考病毒,在新建立的体外模型中研究SIR的作用机制并证实其保护作用。
我们在PERV-C(5683)的基础上开发了三种PERV-C构建体,每种构建体在包膜基因的不同位置(SP-HA, HA-VRA和RPep-HA)携带血凝素标签(HA-tag),以区分原发感染和重复感染。新生成的PERV-C(5683)-HA病毒通过定量病毒RNA、逆转录酶活性、蛋白表达分析和感染研究进行了鉴定。结果表明,SP-HA和RPep-HA与PERV-C(5683)具有相当的复制能力,而HA-VRA则不具有复制能力。选择SP-HA和RPep-HA攻击PERV-C(5683)阳性的ST-IOWA细胞,表明PERV-C- ha病毒不能重复感染这些细胞。它们不整合到基因组中,也不表达。
SIR的机制适用于PERV-C。PERV-C颗粒的产生是一种防御外源PERV-C重复感染的机制。新生成的PERV-C(5683)-HA克隆证明了这一点,可以用作前沿工具。PERV- c的ha标记是新颖的,为其他人类热带PERV病毒的标记提供了蓝图。标记的病毒适用于体外和体内感染的进一步研究,并将有助于病毒入侵和发病机制的基础研究。它将保持XTx的病毒安全性。
猪到人异种移植(XTx)是克服人类同种异体移植物有限可用性的一种很有前途的策略[1,2,3]。2022年,人类患者接受了首例转基因猪心脏移植手术[4]。不幸的是,在患者血液中发现了猪巨细胞病毒(PCMV),证实了病毒传播是难以预防的[4,5]。虽然指定无病原体(DPF)育种可以明显地消除大多数猪病毒,但不能排除猪内源性逆转录病毒(PERV)。它们稳定地整合在猪基因组中[6,7,8,9]。多嗜性PERV-A和-B能在体外感染人细胞,而嗜生态型PERV-C仅能感染猪细胞[6,7,8,9,10,11,12,13]。PERV-C引起了人们的关注,因为它可能与PERV-A重组成具有高传染性的人类热带PERV-A/C变体,并以高滴度复制[14,15,16,17]。由于进化年龄的原因,在猪基因组中发现的大多数原病毒PERV位点都是缺陷的[7,18],并且完整的全长序列的数量相对较少[19,20,21,22,23,24,25,26]。考虑了功能失调的原病毒可能重组的假设,但未得到证实。到目前为止,在没有功能性原病毒的细胞中还没有观察到功能性颗粒[7,27]。它强调,功能性PERV的缺失是保证XTx安全的必要条件[28,29,30,31,32,33]。随着2015年使用CRISPR/Cas9对PERV进行全基因组失活[34,35],以及发现失活细胞系(PK15克隆15)对PERV-A, -B, -A/C重复感染(SI)具有抗性,重复感染抗性(SIR)被讨论为一种保护机制[36]。
一般情况下,逆转录病毒在初始(原发)感染后建立干扰机制,防止被感染细胞被类似或同类型病毒重复感染,从而在细胞中产生SIR[37]。SIR可能是由于受体在细胞内或细胞表面与已知病毒糖蛋白相互作用后被隐藏或下调所致[37,38,39,40]。逆转录病毒如小鼠白血病病毒(MuLV)、人类免疫缺陷病毒(HIV)和泡沫病毒(FV)使用env介导的SIR机制,因此PERV可能也有类似的机制[36,37]。研究表明,前病毒基因产物可以介导病毒复制的限制[37]。因此,病毒特异性基因的靶向表达应被视为一种潜在的抗逆转录病毒感染的保护机制。已经发表了几个例子。
1975年,Suzuki发现了Fv4基因,该基因从Fv4位点编码逆转录病毒相关的Env多蛋白,该多蛋白包含中间pol区、Env和3 '长末端重复序列(LTR)[41,42,43]。稳定转染克隆的Fv-4 env基因的NIH 3T3细胞系的体外数据证实了SIR对生态性mulv的影响[44]。使用携带Fv4基因的转基因小鼠进行的体内研究证实了这一结果。抗性与Fv-4 env表达水平相关。据推测,MuLV受体可能被Fv4-Env复合物所掩盖[45]。
对于PERV,在被CRISPR/Cas9灭活的猪肾细胞系(PK15克隆15细胞)中释放出逆转录酶(RT)缺陷的PERV- a和-B,证明了PERV SIR机制的证据[34,36]。这些细胞仍然产生完整但功能失调的病毒颗粒,其形状不规则,明显不成熟[36]。
细胞不能再感染并保持RT阴性。然而,外源PERV-A、-B、-C或-A/C是否能够进入细胞的问题并没有得到充分的回答,因为用于该分析的所有病毒都是未标记的野生型病毒,几乎无法与退去的病毒区分开来。
在本研究中,我们重点研究PERV-C(5683)作为参考病毒。我们首次生成了ha标记的PERV- c病毒,并提供了PERV标记的蓝图。在原代感染和未感染的猪ST-IOWA细胞的体外实验中,对病毒的功能和SI进行了测试。结果表明,最初感染功能性PERV-C(5683)的ST-IOWA细胞随后表现出对同一类型病毒感染的抗性。由于没有与宿主基因组整合,抗性可能会在感染的早期阶段传递。我们的数据证明PERV- c也存在SIR,并且SIR是由功能和功能失调的PERV颗粒介导的。这一发现为利用病毒成分治疗细胞耐药性开辟了新的策略[34,35,36,46,47,48]。此外,标记的病毒是一种新的工具和数据,适合于生成例如PERV-A, -B和-A/C克隆,以进一步分析PERV感染机制,可能在体内。
通过在PERV-C(5683)主链(KY352351.2)的env基因中插入ha序列(YPYDVPDYA)[26],生成了PERV-C(5683)-HA病毒。ha -标签位于(i)信号肽(SP)下游,产生PERV-C(5683)-SP-HA (SP- ha), (ii)可变区A (VRA)上游,产生PERV-C(5683)-HA-VRA (HA-VRA), (iii) r肽(RPep)下游,产生PERV-C(5683)-RPep-HA (RPep- ha)(图1,表1)。通过转染ST-IOWA细胞并随后分析(i)病毒表达,测试了三个ha标记的PERV-C(5683)构建物,即SP- ha, HA-VRA和RPep- ha的功能。(ii) RT活性,(iii)标记的原病毒与宿主基因组的稳定整合,(iv)病毒颗粒的形态以及(v)感染能力。SP-HA和RPep-HA在转染后14天(p.t)表达了PERV-C环境病毒和pol病毒RNA (vRNA)(图2A, B)。vRNA水平与PERV-C(5683)相当,约为106-107拷贝/μL (envC)和105-106拷贝/μL (pol), p.t 56天。HA-VRA显示,在56天时,envC和pol的低表达量约为102和103拷贝/μL,与天然ST-IOWA细胞的基础表达量相当[9]。术后14天检测到RT活性(图2C)。在定量时,PERV-C(5683)、SP-HA和RPep-HA的RT活性保持在相当水平,SP-HA的RT活性为57 mU/mL, RPep-HA为79 mU/mL, PERV-C(5683)的RT活性为67 mU/mL。在第42天达到最大RT活性,SP-HA为78 mU/mL, RPep-HA为102 mU/mL, PERV-C为98 mU/mL(5683)。HA-VRA无RT活性。原生ST-IOWA细胞作为阴性对照(ctr?)。
图1
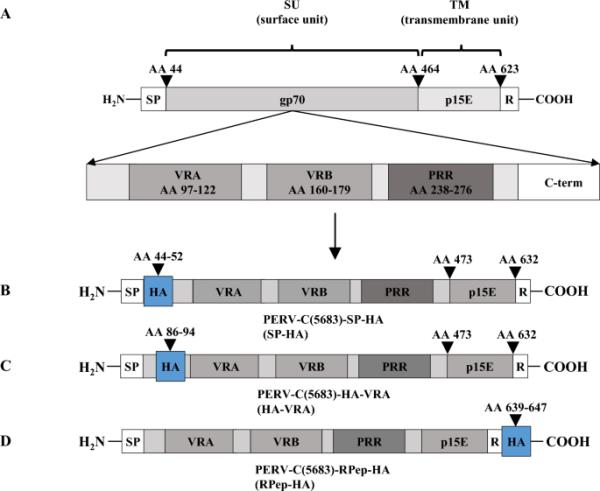
PERV-C(5683)-HA结构的结构与设计。通过定点诱变将ha标签插入PERV-C(5683) (KY352351.2)的env基因中。PERV-C(5683) env的规则结构。PERV-C(5683)分子克隆携带ha -标签B C末端到氨基酸(AA) 44-52的SP (SP- ha), C n末端到AA 86-94的VRA (HA-VRA)或D C末端到AA 639-647的RPep (RPep- ha)。HA的整合位点是根据功能研究[9,25,56,57]和使用开源工具PSIPRED[55]进行二级结构分析来选择的。
表1 Oligo用于克隆的核苷酸引物PERV-C(5683)-HA质粒的制备
图2
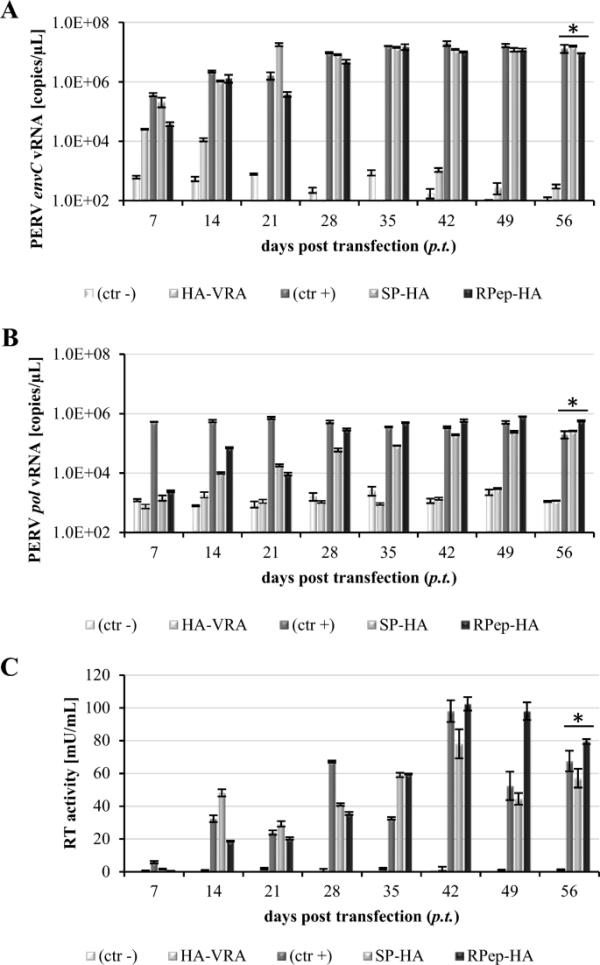
转染ha标记PERV-C(5683)的ST-IOWA细胞中vRNA和RT活性的定量分析。细胞监测56 d,每周收集细胞培养SNs。与阳性对照PERV-C(5683) (ctr+)相比,SP-HA和RPep-HA中PERV-C(5683) A env和B pol vRNA的表达水平相等。HA-VRA转染的细胞仅显示与PERV-C阴性ST-IOWA细胞(ctr?)相当的基础表达。C与vRNA PERV-C(5683)的存在一致,SP-HA和RPep-HA在转染后两周内呈RT阳性。HA-VRA的RT活性仍为阴性。根据Welch’s t检验,显著性均值< 0.05用(*)表示。分析分三次进行
结果表明,在信号肽(SP-HA)或膜锚点(RPep-HA)附近插入ha标签对病毒功能没有影响。将n端引入VRA区抑制病毒复制。由于缺乏vRNA表达,HA-VRA作为原病毒整合到宿主基因组的能力被检测。为此,利用envc特异性引物,对转染HA-VRA的ST-IOWA细胞的基因组DNA (gDNA)进行PCR分析,以确定HA-VRA的整合。没有检测到HA-VRA原病毒整合到宿主基因组中(数据未显示)。因此,HA-VRA被排除在进一步的分析之外。
通过免疫荧光(IF)实验和western blot (WB)分析重组SP-HA和RPep-HA的稳定ha标签整合和蛋白表达(图3)。IF显示转染的ST-IOWA/SP-HA和ST-IOWA/RPep-HA细胞系中存在EnvC-HA蛋白(图3A)。
图3
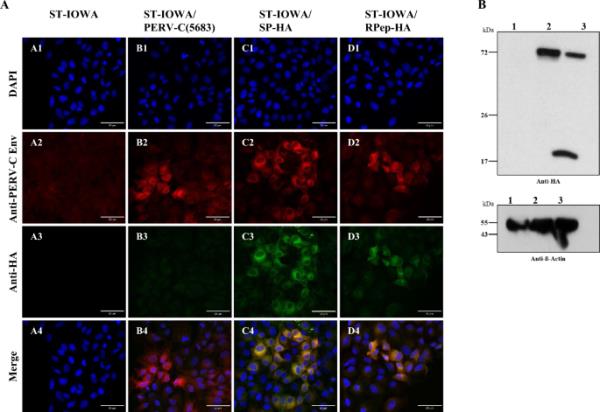
PERV-C转染ST-IOWA细胞的免疫荧光和WB分析。用抗ha标签和抗envc定向抗体转染ST-IOWA细胞56天后的免疫荧光分析。A1-4: ST-IOWA细胞(ctr?),B1-4: PERV-C(5683)阳性ST-IOWA细胞(ctr+), C1-4: SP-HA和D1-4: RPep-HA转染ST-IOWA细胞。除未转染的对照ST-IOWA外,所有细胞均检测到PERV-C Env蛋白(红色荧光)。绿色荧光显示,PERV-C Env-HA蛋白仅在转染SP-HA或RPep-HA的细胞中观察到。B在ST-IOWA细胞裂解液中通过WB分析检测HA蛋白,ST-IOWA细胞转染SP-HA或RPep-HA于第56天收获(车道1:ST-IOWA (ctr -),车道2:SP-HA和车道3:RPep-HA)。Anti - β - actin作为负载对照。PERV-C Env-HA前体预计为72.1 kDa,其裂解产物SP-HA-SU为52.3 kDa, TM-HA为20.9 kDa。检测到PERV-C Env-HA前体蛋白SP-HA和RPep-HA。与前体蛋白相比,SP-HA-SU仅表现出轻微的大小变化。对于RPep-HA,检测到前体和裂解产物
使用抗ha标签抗体的WB分析证实EnvC-HA作为前体存在,并以其加工形式存在,即表面单元(SU)和跨膜单元(TM)(图3B)。根据ha标签位置的不同,对被切割变异的检测要么是限制在SU的n端,要么是限制在TM的c端。正如预期的那样,SP-HA (lane 2)在大约70 kDa处显示一个大的蛋白带,代表前体EnvC-HA (72.1 kDa)。前驱体和SP-HA-SU (52.3 kDa)不能区分。对于RPep-HA,检测到前体EnvC-HA (72.1 kDa)和TM-HA (20.9 kDa)。
电子显微镜(EM)显示,ha标签的整合没有改变病毒颗粒的形态(图4)。SP-HA和RPep-HA的EM显示了病毒颗粒的特征形态,显示密集,塌陷的核心被均匀圆形的衣壳包围,与天然PERV-C(5683)相当。ST-IOWA细胞的EM未显示任何病毒或病毒样颗粒(数据未显示)。
图4
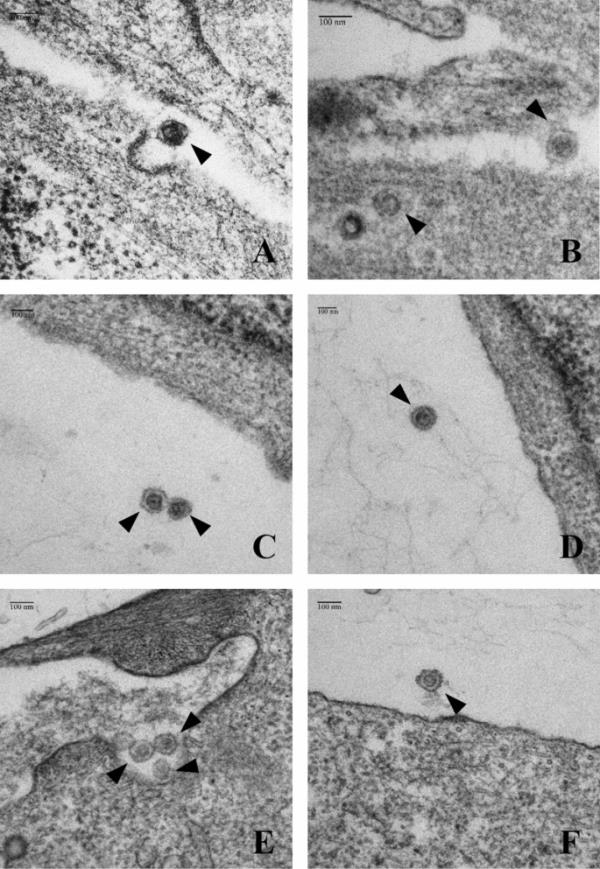
PERV-C病毒颗粒在转染ST-IOWA细胞中的电镜观察。A、B PERV-C(5683)颗粒,C、D病毒在SP-HA转染ST-IOWA细胞中,E、F病毒颗粒在RPep-HA转染ST-IOWA细胞中。病毒粒子用黑色箭头表示。所有的病毒颗粒都表现出相同的形态:致密、塌陷的核被均匀圆形的衣壳包围
接着,PERV-C- ha病毒SP-HA和RPep-HA的功能通过将原生ST-IOWA细胞与含有转染细胞系上清(SN)的病毒孵育得到证实(表2)。ST-IOWA细胞感染ST-IOWA/PERV-C(5683)细胞的SN作为阳性对照。通过对PERV- c env和PERV pol vRNA表达、RT活性测量和IF的量化,每周监测感染进展(图5)。无论用于感染的PERV- c变异,从第二周开始观察到vRNA表达达到105-106拷贝/μL(图5A, B),从第三周开始检测到RT活性在15 - 50 mU/mL之间(图5C)。此外,在感染后第56天(p.i),使用抗ha标签抗体和抗envc肽定向抗血清,用IF区分感染和非感染细胞(图5D)。
表2用于ST-IOWA感染和ST-IOWA/PERV-C(5683)细胞重复感染的PERV-C产生细胞系
图5
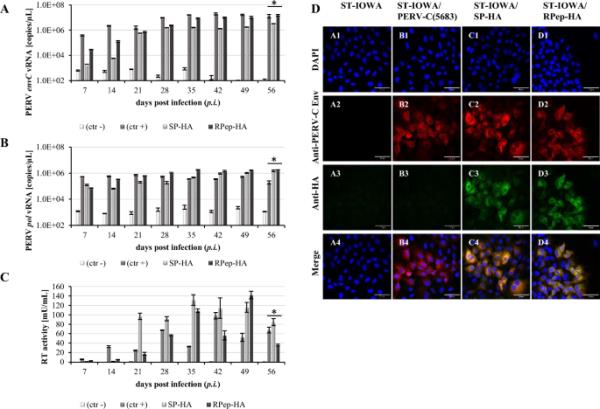
用ha标记的PERV-C(5683)细胞培养SN感染ST-IOWA细胞。细胞与SN孵育24 h,每周监测感染56 d。A envC和B pol vRNA定量显示,作为阳性对照的PERV-C(5683)以及SP-HA和RPep-HA的拷贝数从第一周开始增加。未感染的ST-IOWA细胞保持在基础表达水平。C定量RT活性。除作为阴性对照(ctr?)的未感染ST-IOWA细胞外,所有细胞系从第14天起均可检测到RT活性。D使用PERV-C Env和ha标签定向抗体对感染ST-IOWA细胞第56天进行免疫组化。A1-4 ST-IOWA (ctr?),B1-4 PERV-C(5683)感染ST-IOWA细胞(ctr+), C1-4 SP-HA感染ST-IOWA细胞,D1-4: RPep-HA感染ST-IOWA细胞。根据转染研究,PERV-C Env-HA仅存在于SP-HA或RPep-HA感染的ST-IOWA细胞中,以绿色和黄色表示。根据Welch’s t检验,三个重复< 0.05的显著性平均值用(*)表示。
使用AlphaFold2软件对PERV-C(5683) Env以及三种ha标记的EnvC进行结构分析和比较[49],以深入了解PERV-C Env结构可能发生的变化,从而导致功能性或非功能性病毒。
在这里,通过MUSCLE序列比对对原生EnvC和标记的EnvC- ha变体的预测结构进行了比较(图6)。作为一种需要证明的计算预测,在比较模型3的排名001的预测时,结果表明ha标签的整合导致了轻微的构象变化。
图6
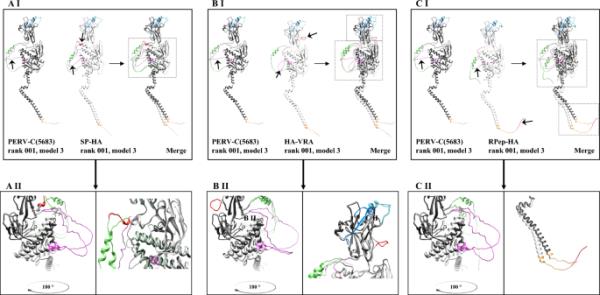
原生PERV-C(5683) (KY352351.2)和ha标记PERV-C(5683)变体的结构预测。使用AlphaFold2预测结构[46],并使用MUSCLE比对进行比较。PERV-C(5683)为深灰色,PERV-C(5683)-HA变体为浅灰色。主要的序列基序是用颜色编码的SP(绿色)、VRA(浅蓝色)、VRB(深蓝色)、PRR(紫色)和RPep(黄色)。ha标签为红色。PERV-C(5683)与SP-HA的比较与比对。AI:全蛋白质。预测结构变化的详细视图。在SP- ha中插入ha标签导致PRR的移位(左),并在SP附近形成一个额外的α螺旋(右)。B PERV-C(5683)和HA-VRA的比较和比对。(B I)全蛋白质。(B II),预测结构变化的详细视图。在HA-VRA中观察到PRR的扭曲,与PERV-C(5683)(左)相比,导致压缩循环。此外,ha标签形成了一个本质扭曲的环(右)。PERV-C(5683)与RPep的比较与比对。全蛋白。预测结构变化的详细视图。与PERV-C(5683)相比,RPep-HA的结构略有移位。主要区别在于SP、PRR(左)和RPep(右),并以箭头表示。pLDDT分数显示在附加文件3:图S3
考虑pLDDT分数(< 50),SP- ha和RPep-HA的轻微结构变化如SP和脯氨酸富区(PRR)的轻微构象位移未被考虑。有趣的是,与野生型相比,两种构建体都显示了TM (p15E)的小转化,pLDDT得分在40到90之间(图6AI, AII, CI, CII)。对于无功能变异HA-VRA,结构预测显示SP (AA 1-43)和TM (AA 473-623)的结构与PERV-C(5683)几乎相同。然而,VRA上游的引入导致HA-tag (AA 86-94)形成本质扭曲环(pLDDT评分< 50)。此外,PRR (AA 247-285)发生了重大的结构变化(pLDDT评分< 50)。PERV-C(5683)的PRR由宽环区组成,而HA-VRA PRR的改变导致扭曲,从而以不同角度放置压缩环(图6 B I, B II)。
PERV-C-HA变异的比对(附加文件2:图S2)表明,SP-HA和RPep-HA也观察到类似的变化,而HA-VRA与其他变异的差异更大。虽然在TM中仅发现微小差异(附加文件2:图S2 A),但在SP(附加文件2:图S2B)和PRR(附加文件2:图S2C)中观察到显著差异。
为了进行PERV-C SIR分析,用PERV-C(5683)-HA病毒(SP-HA或RPep-HA)攻毒ST-IOWA/PERV-C(5683)细胞,建立重复感染(SI)。随访56 d。采用qRT-PCR(图7A-C)、RT活性测定(图7D)、IF(图8A)和WB分析(图8B)进行分析。作为病毒感染性(即功能)的对照,原生ST-IOWA细胞被相同的接种物成功感染。对于实验读数,采用qRT-PCR定量检测PERV envC vRNA的表达(图7A)。由于SI细胞和原代感染细胞都表达带有或不带有ha标签的PERV-C env,因此PERV-C env vRNA表达水平保持稳定(106-107拷贝/μL)。通过随后使用envC-HA特异性寡核苷酸的qRT-PCR区分原发性和继发性感染(表3)。与对照组相比,结果显示SI细胞中没有表达。原发感染的ST-IOWA对照细胞envC-HA vRNA为105-106拷贝/μL,继发感染的SI ST-IOWA/PERV-C(5683)细胞envC-HA vRNA为102-103拷贝/μL(图7B, C)。RT活性测定用于监测感染细胞的逆转录病毒酶活性,结果显示所有细胞均为RT阳性(图7D)。结合PERV-C Env肽和ha特异性抗体,通过IF(图8A)和WB(图8B)分析EnvC和EnvC- ha蛋白表达的存在。PERV-C Env蛋白在除ST-IOWA (ctr?)细胞外的所有细胞中均检测到。HA蛋白仅在原代感染对照中检测到,而在SI细胞中未检测到。数据证实,标记的病毒具有感染原生ST-IOWA细胞的能力,然而,它们不会重叠感染原代感染的ST-IOWA/PERV-C(5683)细胞。
图7
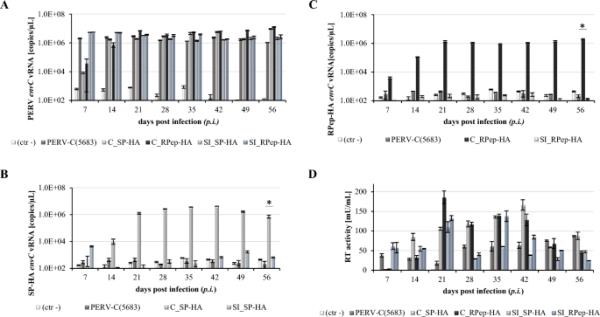
用PERV-C(5683)-HA病毒攻毒ST-IOWA/PERV-C(5683)后vRNA和RT活性的定量分析利用A envC和B、C envC- ha特异性引物,采用qRT-PCR检测PERV-C env vRNA的表达。D酶活性检测采用RT法。采用原生ST-IOWA细胞作为阴性对照(ctr?),感染PERV-C(5683)-HA的ST-IOWA细胞作为阳性对照,以确认病毒的功能。从第7天开始,在除ST-IOWA (ctr?)外的所有细胞中检测envC vRNA的表达。在含有细胞培养SNs的SP-HA或RPep-HA感染的ST-IOWA细胞中检测到B、C envC-HA vRNA,但在PERV-C(5683)-HA攻击的PERV-C(5683)-HA阳性细胞中检测不到vRNA。根据Welch’s t检验,显著性均值< 0.05用(*)表示。分析分三次进行
图8
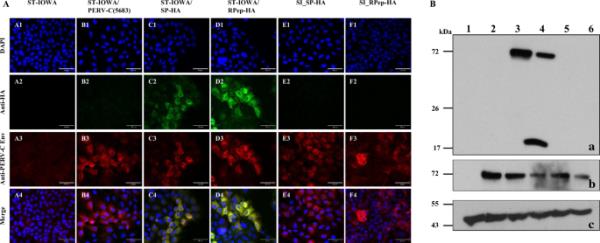
重复感染后的免疫荧光和WB分析。PERV- c(5683)阳性ST-IOWA细胞使用针对PERV- c Env和HA-tag的抗体重复感染后PERV蛋白的免疫荧光。在第56天监测蛋白表达。A1-4:未感染ST-IOWA (ctr?),B1-4: PERV-C(5683)阳性ST-IOWA细胞(ctr+), C1-4: SP-HA (ctr+)或D1-4: RPep-HA (ctr+)感染的ST-IOWA细胞,E1-E4: SP-HA或F1-4: RPep-HA重复感染的ST-IOWA细胞。在除(ctr?)外的所有细胞中均观察到PERV-C Env蛋白,而HA蛋白仅存在于原代感染的对照细胞中。B使用针对(a) ha标签或(B) PERV-C Env的抗体对PERV-C蛋白进行WB分析。PERV-C(5683)-HA病毒在ST-IOWA-PERV-C(5683)细胞重复感染56天后行WB检测。以原生ST-IOWA细胞为阴性对照(ctr?)。感染SN病毒的ST-IOWA细胞也用于重复感染,作为阳性对照(ctr+)。车道1:ST-IOWA (ctr?),车道2:PERV-C(5683)阳性ST-IOWA细胞,车道3 - 4:ST-IOWA细胞感染(3)SP-HA (ctr+)或(4)RPep-HA (ctr+),车道5 - 6:PERV-C(5683)阳性ST-IOWA细胞感染(5)SP-HA或(6)RPep-HA。A SP-HA和RPep-HA均检测到EnvC-HA前体(72.1 kDa)。SP-HA-SU对应的裂解产物略低于前驱体,因此用阴影表示。由于ha标签位于RPep-HA的c端,因此只检测裂解产物TM-HA。B为了分化EnvC和EnvC- ha,使用了抗perv - c Env(498)抗血清。除阴性对照外,所有细胞均检测到PERV-C Env蛋白。C抗- β -肌动蛋白WB作为加载对照
表3 Oligo用于qRT-PCR的核苷酸引物
此外,利用PERV-C env和envC-HA特异性引物,通过PCR排除了病毒整合到SI细胞宿主基因组的可能性(表3),分析了感染细胞和SI细胞的gDNA(附加文件4:图S4)。重复感染后未检测到ha标记的前病毒PERV-DNA。
摘要
背景
结果
讨论
结论
方法
数据和材料的可用性
缩写
参考文献
致谢
作者信息
道德声明
补充信息
搜索
导航
#####
PERV的多个原病毒拷贝在猪基因组中传播。其中一些编码功能性PERV,其中只有PERV-A、-B和-A/C能够在体外感染人类细胞。它们在XTx过程中被认为是一种风险。到目前为止,除了猪组织和细胞移植后的微嵌合效应外,没有PERV在体内传播的记录[50,51]。然而,缺乏证据表明多性PERV对人类异种移植受体没有感染潜力仍然是一个障碍。因此,产生无功能性PERV的供体动物并保护它们免受再感染是开发基于猪细胞的治疗方法的必要条件。一种方法是使用CRISPR/Cas9使PERV全基因组失活[34]。一个有益的副作用是,失活的PK15细胞仍然产生失活的病毒颗粒,保持细胞对SI的抗性。这表明PERV RT失活后具有潜在的保护作用,并为如何从PERV SIR中获益提供了初步见解[36]。
为了继续研究,我们制备了ha标记的PERV-C(5683)作为模型病毒,在体外接种PERV-C(5683)阳性的ST-IOWA细胞,并证实SIR对PERV-C也有效。为此,PERV-C(5683)病毒在envC的三个不同区域(SP-HA、HA- vra和RPep-HA)上标记HA序列标签。SP-HA和RPep-HA病毒的传染性与PERV-C相当(5683)。相反,ha标签n端与VRA区域的整合导致病毒感染性受损。这一发现表明该区域的结构重要性受到阻碍,例如,通过破坏结合动机或在整合新氨基酸时干扰蛋白质结构。使用AlphaFold2进行计算分析,证实HA-VRA结构变化导致重组能力丧失。主要变化位于环路区域,预测精度有限(pLDDT评分< 50)。然而,值得一提的是,它们区分了非功能变体HA-VRA与PERV-C(5683)以及功能变体SP-HA和RPep-HA。
对插入突变的响应性标志着VRA上游区域是进一步病毒失活研究的潜在靶点,并且可能适用于其他PERV类别。
PERV ha标记可以区分原发性和继发性感染,如PERV- c阳性ST-IOWA细胞所示。因此,PERV-C SIR被确认。除此之外,ha标记的PERV-C为进一步研究宿主-病原体在体外和体内的相互作用提供了一个有用的工具。已被证明适合PERV-C中标签引入的位置适用于其他PERV类别,例如PERV-A, -B, -A/C。
就SI而言,ST-IOWA/PERV-C(5683)细胞受到同类型病毒攻击而不受影响,这方面提出了有关其机制的问题。无论是病毒蛋白的存在、病毒颗粒的形成,还是功能性病毒本身的释放,似乎都能防止宿主细胞受到相同或类似病毒的新感染。对于PERV-C,已证明标记的病毒没有整合到宿主基因组中。即使SI细胞envC-HA DNA呈阴性,也不能排除病毒RNA进入宿主细胞的可能性。无法整合可能是由于细胞进入不足引起的,例如附着,受体结合或融合,或者由于进入后影响剥离或整合本身的不足。来自MuLV和FV研究的数据[41,45,52]表明逆转录病毒SI在早期被阻断,例如通过env结合掩盖或下调受体,或通过抗病毒因子的普遍上调。对于PERV,期望有一个类似的机制。在PK15和ST-IOWA细胞中,猪PERV-A受体(POPAR)在RNA水平上表达,ST-IOWA细胞显示PERV-A环境RNA的基础表达[36]。PERV-RNA的表达不足以限制SI,这表明在蛋白水平上受到抑制。
因此,PERV蛋白对外源性PERV感染的保护作用是显而易见的。Takeuchi等人,1998年在其宿主范围和干扰研究中证明,活跃产生PERV-A或-B等病毒的细胞对同类假型病毒不敏感[6]。Argaw等人[53]也得出了类似的结果。感染PERV不包括再感染同类PERV。由于不同的宿主受体,感染不同类型的PERV是可能的。由于PERV的向性是由Env蛋白决定的,因此它是最有可能介导SIR的因素。即使描述了非Env介导的SIR机制,例如Gag/MuLV [54,55], PERV似乎也不太可能。gag介导的SIR预计可以保护所有PERV类,因为它高度保守。它的作用方式可能是辅助因子或载体蛋白。
最终,SIR通过再感染阻止宿主基因组中PERV的扩增。另一方面,包括perv在内的ERV可以通过细胞内逆转录转位进行扩增[56,57],通过转录和随后的逆转录导致ERV序列缺失LTR的不同部分。最后但并非最不重要的是,计算机筛选显示,env基因丢失与基因组拷贝数的显著(高达30倍)增加有关,这意味着这种无env的ERV可以被认为是基因组的超传播者[58]。这可能是猪基因组中多个功能失调的PERV拷贝的解释。
新生成的PERV-C(5683)-HA病毒是了解PERV-C宿主-病原体相互作用的合适工具。在SIR基础上应用已有的抗PERV感染的细胞防御机制是一种新的方法,将有助于提高异种移植的病毒安全性。
必须确保消除XTx中的功能性PERV。近年来,通过筛选不含PERV- c的猪和使用CRISPR/Cas9使PERV全基因组失活,在这一领域取得了巨大成功。然而,预防PERV供体动物的再感染(即SI)是重要的。因此,我们开发了ha标记的功能性PERV,证实SIR的机制也适用于PERV- c。它开辟了一种新的可能性,利用现有的自然保护机制来对抗PERV,从而支持XTx的病毒安全性。
从pBluescript SK (+) (Agilent Technologies, Germany)克隆的PERV-C(5683) (KY352351.2)[26]病毒主干开始设计ha标记的PERV-C。使用开源工具PSIPRED对PERV-C(5683)的EnvC进行结构分析[59],以突出显示不具有结构基序的氨基酸部分(附加文件1:图S1A)。只有定义为线圈的序列片段被选择用于标签的整合。避免整合成螺旋或?-股。根据序列比对、结构分析和已发表的功能研究[11,26,53,60],在AA 44-52、AA 86-94或AA 639-647处引入ha标签,分别形成SP-HA、HA-VRA和RPep-HA。相应的序列见附加文件1:S1B-D。
将HA-tag整合到PERV-C(5683)中,使用Q5?site - directed mutagenesis Kit (New England Biolabs, Germany)按照制造商的说明进行定点诱变。使用的引物如表1所示。
PERV-C来源于ST-IOWA生产者细胞系,携带分子克隆PERV-C(5683), KY352351.2。以原生ST-IOWA细胞[9,61]作为阴性对照。这些细胞易受PERV-C感染,并且RT阴性,因为它们不含功能性PERV-A和-B[62]。细胞按先前描述的方法培养[26,63]。表2列出了用于感染实验的含病毒SNs的细胞和相应的RT活性。
对于体外转染,PERV-C DNA是由EndoFree质粒Maxi Kit (Qiagen,德国)纯化的,按照制造商的推荐。转染前24小时,将ST-IOWA细胞接种于6孔培养板(Sarstedt, Germany)中,每孔2 × 105个ST-IOWA细胞。转染使用FuGene?HD转染试剂(Promega, USA),按照制造商的说明书,转染试剂与DNA的比例为3:1。
对于体外感染,在感染前24小时将3个2 × 105个ST-IOWA细胞/孔接种在六孔培养板(Sarstedt,德国)中。根据RT活性值(表2),将细胞与含不同量的具有复制能力的PERV-C的无细胞SN (1 mL/孔)孵育24 h。用2 mL/孔的磷酸盐缓冲盐水(PBS)洗涤细胞3次以去除输入病毒后,细胞进一步培养56 d。PERV-C的表达和RT的活性每周从合并的3个重复的无细胞SN中进行定量。无细胞SN等分液保存在- 80°C直到测试。
根据制造商的说明,使用QIAamp?病毒RNA迷你试剂盒(Qiagen,德国)从无细胞SNs中分离病毒RNA。使用制造商推荐的定量SYBR绿色RT-PCR试剂盒(德国Qiagen公司),在LightCycler?480(瑞士罗氏生命科学公司)中对PERV pol、env-C和env-C- ha进行一步定量RT-PCR。采用引物对EnvC-for2/EnvC-R3_AWG或F/R对PERV-C env和pol vRNA进行检测和定量[36,63]。对于env-C-HA的定量,循环条件如下:RT反应(50°C, 30 min);变性(95℃,15分钟);扩增40次(94°C, 15 s,变性;68℃,30 s,退火;72℃,30 s,伸长率)。熔化曲线分析如下:95℃,10 s, 65℃,10 s,缓慢加热至97℃,连续测量荧光,冷却(40℃,30 s),根据标记位置使用两种不同的前向引物进行envC-HA定量。反向引物特异性结合ha标签,可用于SP-HA和RPep-HA(表3)。选择正向引物的引物结合位点,形成适合qRT PCR的扩增子。
根据方案b的制造商说明,使用内部HS-MN RT试剂盒(Cavidi Ab,瑞典)测量PERV生产者和感染细胞的无细胞SNs中病毒RT的活性。样品分为三份(每份50μL),并测定平均值和标准差。标准稀释系列的RT活性值从0.11 mU/mL到33.97 mU/mL不等。低于此值的RT活度被认为为RT阴性,并定义了检测极限。
转染ST-IOWA细胞的细胞裂解液经WB分析是否存在结构蛋白。简单地说,样品经过SDS - PAGE(10%)处理,并转移到Immobilon - P PVDF膜(Merck Millipore,德国)上。为了分析ha标记的PERV-C(5683)病毒的功能,用含有5% (w/v)脱脂牛奶的0.1% TBS‐T (AppliChem,德国)阻断膜,用兔抗PERV-C(498)抗血清(1:250)检测蛋白(肽序列:H2N-TGQRPPTQGPGPSSNI-COOH,由Eurogentec,比利时生产)在含5% (w/v)脱脂牛奶(AppliChem,德国)的0.1% TBS‐T中室温保存1小时。使用多克隆兔抗PERV-C(498)抗血清(1:250)和小鼠抗HA抗体(1μg/mL) (Genscript,美国)在含5% (w/v)脱脂牛奶(AppliChem,过氧化物酶偶联驴抗兔(Dianova,德国);1:15 000)或山羊抗鼠(德国Dianova);1:10 000)二抗在0.1% TBS-T中室温孵育1 h。Anti - β - actin(美国Abcam公司);1:10 000)作为对照。检测使用Amersham Hyperfilm?和ECL Western Blotting检测试剂(GE Healthcare, USA)。
使用IF显微镜检测PERV颗粒的方法如前所述[64,65]。简单地说,将半融合到融合的细胞接种在玻璃罩上,用2%甲醛(4% ROTI?Histofix (Carl Roth, Germany) in PBS)在PBS中固定30-45分钟。玻璃罩在4-8°C保存直至使用。用0.5% Triton X-100 (Sigma-Aldrich,美国)孵育10分钟,使细胞渗透。PBS洗涤3次,用1% BSA在PBS中阻断10分钟,用PERV-C(498)抗血清孵育30分钟。用cy3偶联抗兔IgG (Dianova,德国)检测。加入fitc偶联抗ha抗体,与cy5偶联抗兔IgG (Dianova,德国)孵育。样品包埋在含有4′,6-二氨基-2-苯基吲哚二盐酸(DAPI) (Sigma-Aldrich,美国)的Fluoroshield?安装介质中,使用Revolve 4显微镜(ECHO,美国)获取图像。
PERV-C-HA细胞的EM按照前面描述的标准程序进行[21]。简单地说,细胞在室温下用2.5%戊二醛(Sigma - Aldrich, USA)在培养基中固定45分钟。用PBS洗涤细胞2次。随后,在Paul-Ehrlich研究所的电子显微镜设备中进行样品制备。从培养瓶中刮下细胞,与2%温热琼脂糖液体轻轻混合。冷却和凝胶化后,将含有细胞的琼脂糖块切割,用2%四氧化锇(Sigma - Aldrich,美国)在PBS中固定,并用1%单宁酸(Carl Roth,德国)处理。细胞在一系列乙醇浴中逐渐脱水,并包埋在环氧树脂中(Sigma - Aldrich, USA)。在60°C下聚合48 h,然后切割超薄切片,用2%醋酸铀酰(Merck,德国)染色15分钟,然后用2%柠檬酸铅(Serva,德国)染色5分钟。切片在Jeol JEM 1400 Flash电子显微镜下使用电子过滤(ESI)模式检查。
前病毒PERV-C-HA在重复感染细胞后用纯化的gDNA进行PCR分析。按照制造商的推荐,使用QIAamp?DNA Blood Mini Kit (Qiagen, Germany)纯化靶细胞gDNA。用100 ng gDNA进行PCR,引物对PERV-C(5683)-SP-HA为EnvC for3和rvEnvC-HA,引物对PERV-C(5683)-RPep-HA为EnvC for4和rvEnvC-HA。用引物EnvC for3和EnvC- r3_awg进行EnvC特异性PCR作为对照。ST-IOWA细胞的gDNA作为阴性对照。Q5 DNA聚合酶(NEB,德国)按照制造商说明使用。
PERV-C(5683) Env以及生成的ha标记envc的结构预测是通过ColabFold管道使用AlphaFold2进行的,使用的大多是默认参数[49,66]。AlphaFold2提供了一种计算方法,已被用于预测许多蛋白质结构,几乎具有实验精度[49]。使用Chimera对每种蛋白质获得最高模型置信度的结构模型进行结构变化分析[67]。AlphaFold预测后得到的pLDDT分数如附加文件3:图S3所示。
RNA样本采用Welch’s t检验,以0.05为阈值。
下载原文档:https://link.springer.com/content/pdf/10.1186/s12977-023-00630-x.pdf